14. Az oxigén piros?
Szükséges anyagok és összetevőik:
-
Összetevők:
-
Összetevők:
Az oxigén, ahogyan nem ismerjük.
Anyagok: klórgáz, 20 g nátrium-hidroxid 140 cm3 vízben oldva, 30 cm3 30%-os (m/m) hidrogén-peroxid-oldat, jég.
Eszközök: védőszemüveg, 50 és 250 cm3-es főzőpohár, mérőhenger, gázmosópalack, üvegfritt.
A kísérlet végrehajtása: A 250 cm3-es főzőpohárba öntjük a nátrium-hidroxid-, az 50 cm3-esbe a hidrogén-peroxid-oldatot és jeges vízben alaposan lehűtjük. A két oldatot egy gázmosó-palackba öntjük és Kipp-készülékből vagy palackból nyert klórgázt vezetünk át rajta, miközben a helyiséget besötétítjük.
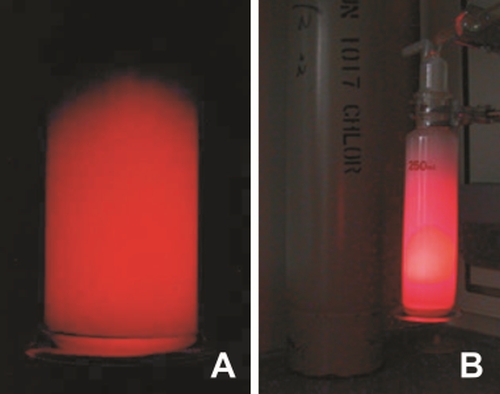
Tapasztalat: A klórgáz bevezetésére az oldat vörös színű lesz. Ez legintenzívebben a gázbevezetés helyén, az üvegfritt környékén látható és a gázbevezetés megszűntével rövid idő után eltűnik.
Magyarázat: „Az oxigén színtelen, szagtalan gáz...” – olvashatjuk a legtöbb könyvben, vagy mégsem mindig? Ha lúgos hidrogén-peroxid oldatába klórgázt vezetünk, az oxigén egy különlegesen aktív formájával találkozhatunk. Ekkor az alábbi reakciók játszódnak le: (1) Cl2 + 2 OH- = OCl- + Cl- + H2O; (2) H2O2 + OCl- = ClOO- + H2O; (3) ClOO- = 1O2 + Cl-; (4) 1O2 = 3O2 + hν. A peroxohipoklorition (ClOO-) bomlásából keletkező ún. szingulett oxigén (1O2) piros szín kibocsátása közben alakul át az általunk ismert színtelen, ún. triplett formává (3O2). Gáz halmazállapotban a szingulett oxigén nagyon hosszú ideig életképes (72 perc), de oldatban ez a másodperc töredékére csökken. Magas koncentrációban két szingulett oxigénmolekula ütközéséből vörös fluoreszcenciát észlelhetünk 634 nm hullámhosszon, ezt láthatjuk a fenti kísérletben is. A két fajta oxigén tulajdonságai jelentősen különböznek, a szingulett oxigén lényegesen reaktívabb. A napfény számos szerves anyagra (pl. polimerekre) gyakorolt károsító hatása a szingulett oxigén jelenlétére vezethető vissza. A szingulett oxigén az ún. reaktív oxigénrészecskék (szuperoxid gyökanion, hidroxilgyök, hidrogén-peroxid, ózon) közé tartozik és részt vesz az endogén (azaz a szervezeten belül keletkező) ózon termelésében is.
Biztonsági tudnivalók és hulladékkezelés: Viseljünk védőszemüveget a kísérlet során. A klórgáz használata miatt a kísérletet vegyifülkében vagy a szabadban végezzük. A nátrium-hidroxid maró, lúgos anyag, oldása hőfejlődéssel jár! Ha bőrre vagy szembe kerül a lúgos oldat, vízzel alaposan öblítsük le/ki, a bőrön híg ecetsavval, a szemben híg bórsavoldattal közömbösítsük és forduljunk szemorvoshoz. A hidrogén-peroxid irritálja a bőrt és a szemet, különösen tömény oldatban. A leggyakoribb probléma a bőrre jutó hidrogén-peroxiddal, hogy kifehéríti a bőrt, de ez rendszerint néhány nap után minden különösebb kezelés nélkül elmúlik, mert a bőr lehámlik. A kísérlet lejátszódása után megmaradt anyagok ártalmatlanításához a teljes reakcióelegyet közömbösítés után kevés kálium-jodiddal kezeljük a hidrogén-peroxid elbontására, majd a lefolyóba önthetjük.
